

凍存通常是指將細胞冷凍儲存在-196℃的液氮中。如在不加任何保護劑的情況下,直接對細胞加以凍存,會導致細胞內、外的水分迅速形成冰晶,進而對細胞結構與功能造成一系列的損害,如機械損傷、蛋白質變性、電解質升高等,最后可引起細胞死亡。為了避免細胞內冰晶的形成,在凍存細胞時常向培養液中加入適量的二甲亞砜(DMSO),因其相對分子質量較小而溶解度大,較易穿透進入細胞中,使細胞內冰點下降,并可提高細胞膜對水的通透性,配合以緩慢冷凍的方法,可使細胞內的水分逐步地滲透出胞外,避免了冰晶在細胞內大量的形成。
復蘇是指將凍存的細胞從-196℃的液氮中取出融解,使其活力恢復的過程。快速融化的手段可以保證細胞外結晶在很短時間內融化,避免由于緩慢融化使水分滲入細胞重新結晶對細胞造成損害。復蘇成功的細胞可以保持很高的活力。

細胞的凍存:
1.用0.25%胰蛋白酶溶液消化處于對數生長期的單層培養細胞,收集消化的細胞于15mL離心管中;
2.800-1000rpm離心5min,棄上清;
3.加入適量凍存液(百澳博無DMSO細胞凍存液),用吸管吹打細胞制懸,調整細胞密度為5×106-1×107個/mL;
4.每個凍存管分裝細胞懸液1mL,旋緊凍存管的蓋;
5.在凍存管上標明細胞的名稱、凍存時間、凍存人名等;
6.將凍存管置于如下條件下逐步加以凍存:-80℃,12h→液氮;
7.若使用含10%DMSO和10%FBS的培養液凍存細胞,則將凍存管置于如下條件下逐步加以凍存:4℃,1h→-20℃,2h→-80℃,12h→液氮。
細胞復蘇和活率測定:
1.用止血鉗從液氮罐凍存盒中取出細胞凍存管1只,迅速將其置入37℃水浴中,不斷搖動使凍存的細胞懸液盡快融化;
2.用酒精棉球擦拭凍存管,放入超凈工作臺中;
3.將已融化的細胞懸液用吸管移入離心管中,加10倍體積的RPMI 1640培養基(含10%小牛血清),吹打混勻;
4.800-1000rpm離心5min,棄上清液;
5.加入培養液吹打沉淀的細胞,使其懸浮,將細胞懸液與0.4%的臺盼藍溶液以9:1的比例混合。?在室溫下染色3-5分鐘,對細胞進行計數,計算活細胞比例;
6.按1×105個mL的細胞濃度,將細胞接種在培養瓶中,置于培養箱中培養;
7.24h后取出培養瓶,觀察細胞生長狀況。

注意事項:
1.對數期的細胞增殖能力強,凍存后生存率較高,因此,在進行細胞凍存時,應盡量選擇處于此期的細胞加以凍存;
2.為了保證凍存的質量及復蘇后細胞的存活率,凍存時應掌握好消化時間,消化過度將對細胞造成損傷,復蘇時細胞難于存活。此外,復蘇后接種時,細胞的濃度不能太低,最好控制在1×105-5×105個/mL,這樣才能保證復蘇成功;
3.凍存管的管蓋應封蓋嚴密,以免復蘇時細胞外溢;
4.復蘇時,從液氮取出凍存管到水浴中融化的過程要快,否則將會導致冰晶的形成,傷害細胞。同時,一次復蘇的凍存管數量不要太多,否則會引起水浴鍋中傳熱不佳,延緩凍存的細胞懸液融化的時間;
5.為防止液氮凍傷,在復蘇過程中應戴上棉質手套。
細胞增殖情況:
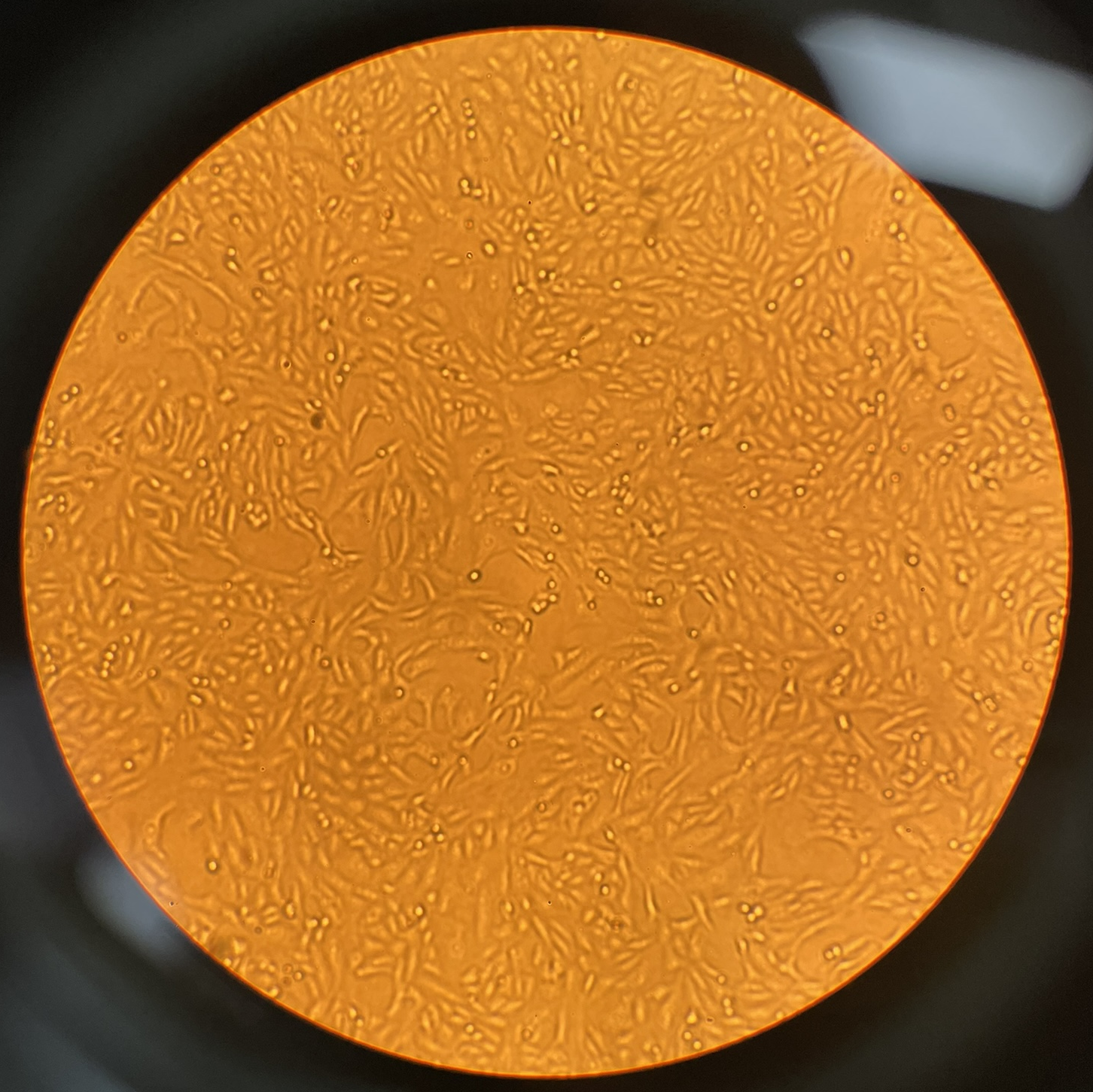
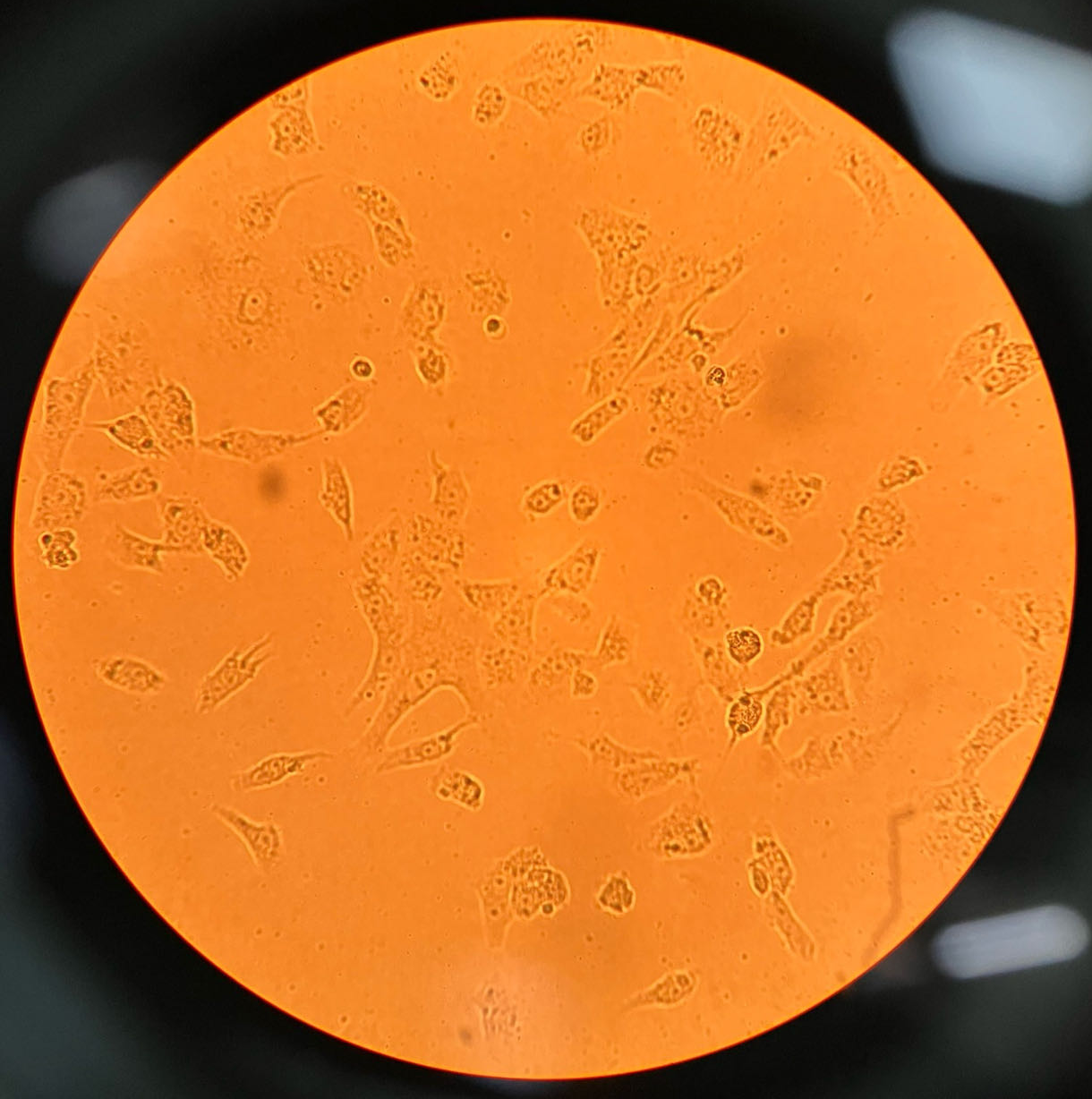
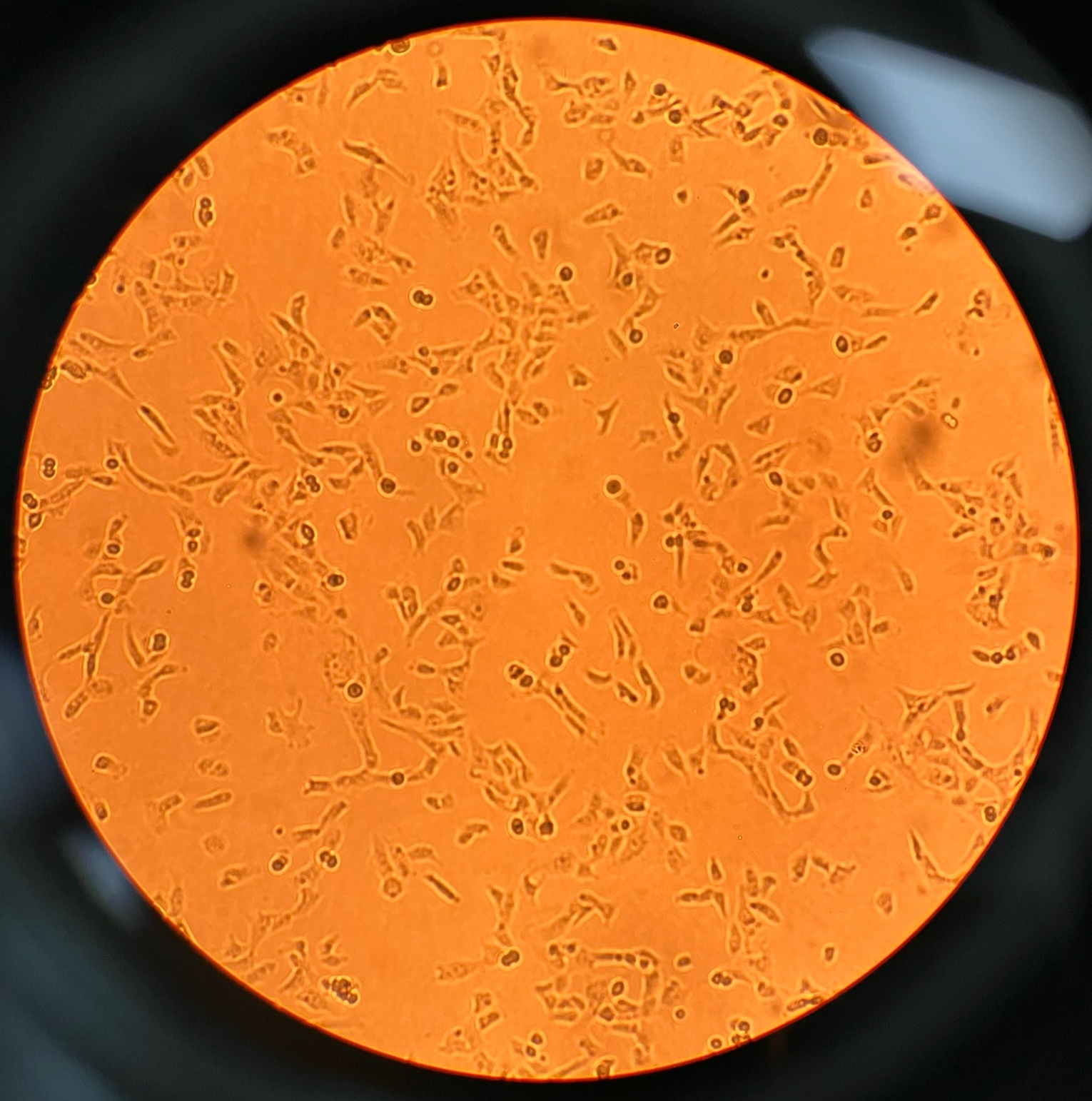
24h貼壁狀態 48h增殖情況 72h增殖情況(細胞匯合度達90%)
|
上一條:使用指南--細胞培養耗材
下一條:實驗小知識--如何進行正確的細胞計數實驗? |
返回列表 |