

【實驗原理】
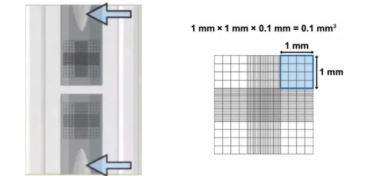
細胞計數板的中央有兩個細胞計數池,上面有激光蝕刻形成的網格;網格由9個主要方格構成,角上的4個方格進一步分成16個較小的方格,中央的主要方格被分為25個較小的方格,每一個較小方格被進一步分為16個微型方格,在每個細胞計數池的遠端是上樣口,待計數的細胞懸液從此處加入。通過計算出一定體積細胞懸液中的細胞數目換算出每毫升細胞懸液中的細胞數。
【實驗步驟】
Step1
制備細胞懸液:
①貼壁生長的細胞,使用胰酶消化的方法使細胞從培養瓶表面脫落;
②漩渦混勻或使用移液器反復吹吸細胞懸液,盡量減少細胞團簇;
③懸浮細胞則可以直接進行取樣計數;
④細胞懸液的計數濃度:5×105個細胞/mL -5×106個細胞/mL。
注意:
1.盡量少、盡量小的細胞團簇;
2.如需計算活率,則需將細胞懸液按照1:1的比例加入等量的0.4%的臺盼藍染料,混勻后,靜置1~2分鐘。
Step2
2.用純水和75%乙醇清洗血細胞計數板表面和蓋玻片,然后用洗耳球吹干,在血細胞計數板的計數池上方蓋上專用的蓋玻片;
注意:最好不要擦拭血細胞計數板的計數池,防止標示線損壞。
Step3
吸取10ul細胞懸液沿著蓋玻片一側緩慢滴加,使細胞懸液填充蓋玻片與計數板之間,注意蓋玻片下不能有氣泡,亦不可讓懸液滴入旁邊凹槽中;
Step4
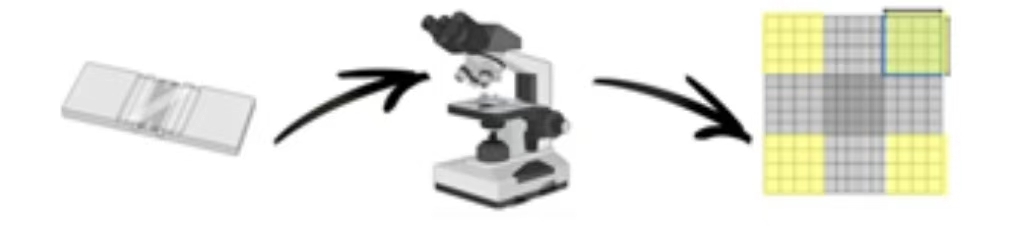
將細胞計數板置于普通顯微鏡下(10×4)觀察,統計血球計數板的四大格中細胞的總數,壓線細胞遵守“計左不計右,計上不計下”的原則;
Step4
細胞懸液中的細胞數目按照以下公式計算:
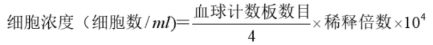
【注意事項】
1.取樣計數前,充分混勻細胞懸液,減少測量誤差;
2.若大方格內細胞數過多,應當對細胞懸液進行適當稀釋后再計數;
3.若每個大方格內的細胞數目相差20個以上,表示細胞分布不均,必須對細胞懸液混勻后重新計數;
4.若顯微鏡下見有兩個或以上的細胞組成的細胞團,則需按單個細胞計算,若出現多個細胞團,可能原因為細胞懸液未充分混勻或稀釋倍數不夠,需要重新混勻或適當稀釋后再次計數;
5.一個細胞計數板有兩個細胞計數池,為了避免誤差,可重復計數,取平均值。
|
上一條:干貨分享--細胞的凍存、復蘇以及活率測定
下一條:好物推薦--多聯插板 |
返回列表 |